Investigacion en Bioquimica Molecular y Proteómica 2008
Por cuarto año consecutivo los alumnos del ultimo año de la especialidad Quimica de la escuela ORT Argentina realizaran sus proyectos finales en distintas universidades y centros de investigacion con profesionales reconocidos. La metodologia de trabajo evita la transposicion didactica permitiendo a los estudiantes realizar su actividad final en los lugares donde se esta generando el conocimiento.
La articulacion entre nivel medio y el posgrado es auspiciada por el CONICET (Consejo Nacional De Investigacion Cientifica...).
Los proyectos de investigacion para el año en curso son:
1) Evaluacion de la expresion de la molecula de adhesion Cadherina epitelial en tejidos humanos normales y tumolares.
Investigador:Doctora monica Vazquez-Levin.
Instituto de Biologia y Medicina Molecular ( IBYME-CONICET).
Alumnos: Yael Dobzewicz y Gala Szapiro.
Link:
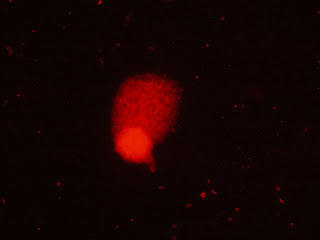
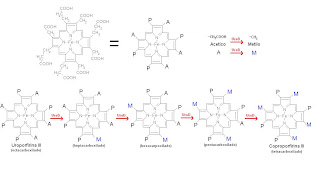
http://www.proyecto-6q.blogspot.com/2) Accion del Hexaclorobenceno (HCB) sobre la Uroporfirinogeno Decarboxilasa de una linea celular de Hepatocitos humanos. Mecanismo de accion.
Investigador:Doctora Maria del Carmen Rios de Molina.
Instituto: Departamento Quimica Biologica, Facultad de Ciencias Exactas y Naturales.
Alumnos: Lucas Toiw y Uriel Frid.
Link:
http://www.proyectofird-toiw08.blogspot.com/3)Modelos experimentales de enfermedades metabólicas: Porfiria y Síndrome Metabólico. Proteómica y Metabolómica de estos disturbios.
Investigador: Dra. Marta Blanca Mazzetti.
Instituto: Departamento de Química Biológica, Facultad de Ciencias Exactas y Naturales (UBA). Alumnos: Maria Duperron y Mauro Elencwajg.
Link:
http://proyectofinal6q.blogspot.com/4) Factores no hemodinámicos relacionados con la génesis y evolución de la proteinuria durante la enfermedad renal progresiva.
Investigador: Dra. Elsa Zotta.
Instituto: Laboratorio de Fisiopatogénia, Departamento de fisiología, Facultad de medicina, UBA. Alumnos: Barbara Helueni y Melanie Naiman.
Link:
http://proyectoq08.blogspot.com/5) Estudio de la participacion de la anandamida en la regulacion de la interaccion espermatozoide-ovioducto en un modelo bovino.
Investigador: Dra. Silvina Perez Martinez.
Instituto: Facultad de medicina - UBA
Alumnos: Judith Arenas Tenenbaum y Melina Braverman
Link:
http://www.scienceproject08.blogspot.com/6) El estudio de los mecanismos moleculares involucrados en la regulación del gen UGA4 de Saccharomyces cervisiae en respuesta a cambios en la disponibilidad de nutrientes con el fin de dilucidar las distintas cascadas de señales desencadenadas por dichos nutrientes y establecer sus interconexiones.
Investigador: Dra Susana Correa García.
Instituto: Departamento de Química Biologica, Facultad de ciencias Exactas y Naturales, Universidad de Buenos Aires.
Alumnos: Iván Mikiej y Victoria Salama
Link:
http://www.proyectoquimica22.blogspot.com/7) Diagnóstico de la enfermedad de Von Willebrand (VWD) tipo 2N por técnicas fenotípicas y genotípicas.
Investigador: Dra. Adriana I. Woods.
Instituto: Instituto de Investigaciones Hematológicas "Mariano R. Castex" de la Academia Nacional de Medicina.
Alumnos: Abigail Skverer y Daniela Lin
Link:
http://www.vwd-diagnostico.blogspot.com/8) Estudio de la mielinogenesis en el sistema nervioso periferico en condiciones fisiologicas y patologicas. Participacion de celulas pluripotentes en el proceso de degeneracion-regeneracion nerviosa.
Investigador: Dra Patricia Setton-Avruj.
Instituto: Dpto de Quimica Biologica, Facultad de Farmacia y Bioquimica (IQUIFIB-UBA-CONICET).
Alumnos: Averbuj Daniel y Eitan Rozenszajn.
Link:
http://www.proyectoaverbuj-rozenszajn.blogspot.com/9) Diseño y desarrollo de vacunas antitumorales empleando bacterias y celulas tumorales modificadas con genes inmunomodiladores. Estudio de los mecanismos inmunes inducidos.
Investigador: Claudia I. Waldner y Claudia Mongini.
Instituto: Laboratorio de inmunologia celular y molecular. Centro de Estudios Farmacologicos y Botanicos (CEFYBO. CONICET-UBA)
Alumnos: Amalia Surijon y Maria Belen Tolava Rivero
Link:
http://www.amibeluproyecto.blogspot.com/10) Marcadores Geneticos Asociados al Cáncer
Investigador: Dr.Javier Hernán Cotignola
Instituto: Laboratorio de Cáncer y Apoptosis del Departamento de Quimica Biologica de la Facultad de Ciencias Exactas y Naturales de la Universidad de Buenos Aires.
Alumnos: Ayelén Marano y Solange Perchik
Link:
http://marcadoresgeneticos.blogspot.com/11) Expresion del canal de la conductancia transmembranal de la Fibrosis Quistica (CFTR) en placentas Preeclampticas: posible rol en la regulacion de la actividad de la Acuoporina-9 (AQP9).
Investigador: Dr Alicia E Damiano
Instituto: Catedra de Biologia Celular, Departamento de Ciencias Biologicas, Facultad de Farmacia y Bioquimica (UBA)
Alumnos: Gabriel Colodenco y Martín Sapir.
Link:
http://proyectofinalcs.blogspot.com/12) Proteómica de factores secretados por células de cáncer de mama y mama normal con capacidad inhibitoria de la producción lipídica.
Investigador: Dra.Guerra de Grignoli Liliana Noemi
Instituto: Departamento de Ciencias biologicas. Facultad de ciencias exactas y naturales,UBA-CONICET.
Alumnos: Fabiana Durante y Tamara Broitman.
Link:
http://tyf-proyecto08.blogspot.com/13) Neovascularizaciòn en un modelo murino de inflamaciòn aguda inducida por LPS.
Investigador:Eulalia de la Torre.
Instituto: Facultad de Medicina - Uba - Laboratorio de Inmunofarmacologia
Alumnos: Federico Mauas Walach, Pablo Kuleff.
Link:
http://www.finalproyectort.blogspot.com/14) Interacción de sumo-1 y mage-a2 en la regulacion del oncosupresor p53
Investigador: Martín Monte
Instituto: Facultad de Ciencias Exactas y Naturales (UBA)
Alumnos: Leonel Stermann y Yair Litman
Blog:
http://proyectosumo.blogspot.com/15) Estudio de la Growth Associated Protein (GAP-43), su interacción con la Ubicutina y su participación en el control del ciclo celular en células NIH3T3 transfectadas en forma estable y transiente. Efecto de la Apo-transferrina en la remielización: participación de la vía Notch en la diferenciación oligodendrioglial.
Investigador: Doctora Ana M. Adamo.
Instituto: Departamento de Química Biológica Patológica, Facultad de Farmacia y Bioquímica de la UBA. CONICET.
Alumnos: Rodrigo C. Pampin y Robby Mattes
Link:
http://www.gap-43.blogspot.com/